En este cuarto capitulo sobre la serie del COVID-19 prolongado, queremos en esta oportunidad tratar dos sistemas: el cardiovascular y el neurológico.
Secuelas cardiovasculares
Epidemiología y manifestaciones clínicas.
Durante las etapas iniciales de la pandemia y dados los pocos estudios publicados al respecto, se creía que este coronavirus causaba síntomas netamente respiratorios; sin embargo, a medida que el número de pacientes aumentó, se observó que la enfermedad cardiovascular tenía un papel fundamental en el desarrollo y pronóstico de la infección. Los factores de riesgo más importantes relacionados con mortalidad son la edad y la presencia de comorbilidades, especialmente de tipo cardiovascular. Aunado a esto, en el COVID-19 prolongado se ha observado secuelas en el sistema cardiovascular.
Efectivamente, se ha informó dolor torácico en hasta ~ 20% de los supervivientes de COVID-19 a los 60 días de seguimiento (Carfi, A., et al. J. Am. Med. Assoc. 324, 603–605, 2020; Carvalho-Schneider, C. et al. Clin. Microbiol. Infectar. 27 , 258-263, 2021), mientras que se notificaron palpitaciones y dolor torácico en curso en el 9 y el 5 %, respectivamente, a los 6 meses de seguimiento en el estudio chino de COVID-19 posaguda (Huang, C.et al. Lancet 397 , 220-232, 2021). Se ha observado una mayor incidencia de miocardiopatía por estrés durante la pandemia de COVID-19 en comparación con los períodos prepandémicos (7,8 frente a 1,5-1,8 %, respectivamente), aunque las tasas de mortalidad y reingreso en estos pacientes son similares (Jabri, A. et al. JAMA Netw. Abierto 3, e2014780, 2020). Los datos preliminares con imágenes de resonancia magnética cardíaca (IRM) sugieren que la inflamación del miocardio en curso puede estar presente a tasas tan altas como 60 % más de 2 meses después de un diagnóstico de COVID-19 en un centro de pruebas de COVID, aunque la reproducibilidad y consistencia de estos datos se han debatido (Puntmann, VO et al. JAMA Cardiol. 5 , 1265-1273, 2020). En un estudio de 26 atletas universitarios de competición con infección leve o asintomática por SARS-CoV-2, la resonancia magnética cardíaca reveló características diagnósticas de miocarditis en el 15 % de los participantes y lesión miocárdica previa en el 30,8 % de los participantes (Rajpal, S. et al. JAMA Cardiol. 6 , 116-118, 2021).
Patología y fisiopatología
Los mecanismos que perpetúan las secuelas cardiovasculares en el COVID-19 posaguda incluyen la invasión viral directa, la regulación a la baja de la ECA2, la inflamación y la respuesta inmunológica que afecta la integridad estructural del miocardio, el pericardio y el sistema de conducción. Los estudios de autopsia en 39 casos de COVID-19 detectaron virus en el tejido cardíaco del 62,5 % de los pacientes (Lindner, D. et al. JAMA Cardiol. 5 , 1281-1285, 2020). La respuesta inflamatoria subsiguiente puede conducir a la muerte de los cardiomiocitos y al desplazamiento fibrograso de las proteínas desmosomales importantes para la adherencia de una célula a otra (Gemayel, C., et al. Cardiol. 38 , 1773-1781, 2001; Siripanthong, B. et al. Heart Rhythm 17 , 1463-1471; 2020).
Los pacientes recuperados pueden haber aumentado de forma persistente la demanda cardiometabólica, como se observa en la evaluación a largo plazo de los supervivientes del SRAS (Wu, Q. et al. Sci. Rep. 7 , 9110, 2017). Esto puede estar asociado con una reserva cardíaca reducida, uso de corticosteroides y desregulación del sistema renina-angiotensina-aldosterona (RAAS). Por otra parte, se ha observado que la fibrosis o cicatrización del miocardio y la miocardiopatía resultante de la infección viral pueden provocar arritmias reentrantes (Liu, PP, Blet, A., Smyth, D. y Li, H. Circulation 142 , 68–78, 2020). Adicionalmente, la COVID-19 también puede perpetuar las arritmias debido a un estado catecolaminérgico elevado debido a citocinas como IL-6, IL-1 y factor de necrosis tumoral-α, que pueden prolongar los potenciales de acción ventriculares al modular la expresión del canal iónico de los cardiomiocitos (Lazzerini, PE, et al. Nat. Rev. Immunol. 19 , 63–64, 2019). La disfunción autónoma después de una enfermedad viral, que resulta en el síndrome de taquicardia ortostática postural y taquicardia sinusal inapropiada, se ha informado previamente como resultado de la modulación adrenérgica (Agarwal, AK, et al. Postgrad. Med. J. 83 , 478–480, 2007).
Consideraciones de manejo
Se puede considerar la evaluación clínica y de imagen en serie con electrocardiograma y ecocardiograma a las 4-12 semanas en aquellos con complicaciones cardiovasculares durante la infección aguda o síntomas cardíacos persistentes (George, P. M. et al. Thorax 75, 1009–1016, 2020; Desai, A. D., et al. Curr. Cardiol. Rep. 23, 2; 2020). La evidencia actual no respalda la utilización rutinaria de imágenes cardíacas avanzadas, y esto debe considerarse caso por caso. Las recomendaciones para los atletas de competición con complicaciones cardiovasculares relacionadas con COVID-19 incluyen la abstinencia de deportes competitivos o actividad aeróbica durante 3-6 meses hasta la resolución de la inflamación miocárdica mediante RM cardíaca o normalización de troponina (Hendren, N. S., et al. Circulation 141, 1903–1914, 2020; Maron, B. J. et al. J. Am. Coll. Cardiol. 66, 2362–2371, 2015).
A pesar de las preocupaciones teóricas iniciales con respecto al aumento de los niveles de ACE2 y el riesgo de COVID-19 agudo con el uso de inhibidores de RAAS, se ha demostrado que son seguros y deben continuarse en aquellos con enfermedad cardiovascular estable (Bozkurt, B., et al. J. Card. Fail. 26, 370, 2020; Lopes, R. D. et al. J. Am. Med. Assoc. 325, 254–264, 2021). En cambio, el cese abrupto de los inhibidores de RAAS puede ser potencialmente dañino (Vaduganathan, M. et al. N. Engl. J. Med. 382, 1653–1659, 2020). En pacientes con disfunción ventricular, la terapia médica dirigida por las guías debe iniciarse y optimizarse según la tolerancia (Guzik, T. J. et al. Cardiovasc Res. 116, 1666–1687, 2020). La retirada de la terapia médica directriz dirigida se asocia con una mayor mortalidad en la fase aguda a la fase de post-aguda en un estudio retrospectivo de 3.080 pacientes con COVID-19 (Rey, J. R. et al. Eur. J. Heart Fail. 22, 2205–2215, 2020). Los pacientes con síndrome de taquicardia ortostática postural y taquicardia sinusal inapropiada pueden beneficiarse de un betabloqueante de dosis baja para controlar la frecuencia cardíaca y reducir la actividad adrenérgica (Raj, S. R. et al. Circulation 120, 725–734, 2009). Se debe prestar atención al uso de fármacos como agentes antiarrítmicos (por ejemplo, amiodarona) en pacientes con cambios pulmonares fibróticos después de COVID-19 (Kociol, R. D. et al. Circulation 141, e69–e92, 2020).
 Secuelas neuropsiquiátricas
Secuelas neuropsiquiátricas
Epidemiología y manifestaciones clínicas.
Similar al síndrome post-SARS crónico, los sobrevivientes de COVID-19 han informado un síndrome post-viral de malestar crónico, mialgia difusa, síntomas depresivos y sueño no reparador (Fauci, A. International AIDS conference. YouTube https://www.youtube.com/watch?v=UMmT48IC0us&feature=emb_logo, 2020; Nordvig, A. S. et al. Potential neurological manifestations of COVID-19. Neurol. Clin. Pract. https://doi.org/10.1212/CPJ.0000000000000897, 2020). Otras manifestaciones post-agudas de COVID-19 incluyen dolores de cabeza similares a la migraña (Belvis, R. Headache 60, 1422–1426 (2020); Arca, K. N. & Starling, A. J. SN Compr. Clin. Med. 2, 1200–1203, 2020), a menudo refractarios a los analgésicos tradicionales (Bolay, H., Gül, A. & Baykan, B. Headache https://doi.org/10.1111/head.13856, 2020) y dolores de cabeza de aparición tardía atribuidos a niveles altos de citocinas. En un estudio de seguimiento de 100 pacientes, aproximadamente el 38 % tenía dolores de cabeza continuos después de 6 semanas (Pozo-Rosich, P. In Proc. AHSAM 2020 Virtual Annual Scientific Meeting (Infomedica, 2020); https://www.ahshighlights.com/summaries-podcasts/article/headache-covid-19-a-short-term-challenge-with-long-term-insights). La pérdida del gusto y el olfato también puede persistir después de la resolución de otros síntomas en aproximadamente una décima parte de los pacientes hasta los 6 meses de seguimiento (Huang, C. et al. Lancet 397, 220–232, 2021; Chopra, V. et al. Ann. Intern. Med. https://doi.org/10.7326/M20-5661, 2020; Arnold, D. T. et al. Thorax https://doi.org/10.1136/thoraxjnl-2020-216086, 2020; Garrigues, E. et al. J. Infect. 81, e4–e6, 2020). Se ha observado deterioro cognitivo con o sin fluctuaciones, incluida la confusión mental, que puede manifestarse como dificultades de concentración, memoria, lenguaje receptivo y / o función ejecutiva (Heneka, M. T., Alzheimers Res. Ther. 12, 69, 2020, Ritchie, K., et al. Brain Commun. 2, fcaa069, 2020; Kaseda, E. T. & Levine, A. J. Clin. Neuropsychol. 34, 1498–1514, 2020).
Por otra parte, las personas con COVID-19 experimentan una variedad de síntomas psiquiátricos que persisten o se presentan meses después de la infección inicial (Postolache, T. T., et al. JAMA Psychiatry https://doi.org/10.1001/jamapsychiatry.2020.2795, 2020). En una cohorte de 402 sobrevivientes de COVID-19 en Italia 1 mes después de la hospitalización, aproximadamente el 56 % resultó positivo en al menos uno de los dominios evaluados para secuelas psiquiátricas (TEPT, depresión, ansiedad, insomnio y sintomatología obsesivo compulsiva) (Mazza, M. G. et al. Brain Behav. Immun. 89, 594–600, 2020). Se informó depresión y ansiedad clínicamente significativas en aproximadamente el 30-40 % de los pacientes después de COVID-19, similar a los pacientes con infecciones previas graves por coronavirus (Lam, M. H. et al. Arch. Intern. Med. 169, 2142–2147, 2009; Lee, S. H. et al. Psychiatry Investig. 16, 59–64, 2019; Mazza, M. G. et al. Brain Behav. Immun. 89, 594–600, 2020; Rogers, J. P. et al. Lancet Psychiatry 7, 611–627, 2020). La ansiedad, la depresión y las dificultades para dormir estuvieron presentes en aproximadamente una cuarta parte de los pacientes a los 6 meses de seguimiento en el estudio chino COVID-19 post-aguda (Huang, C. et al. Lancet 397, 220–232; 2021). En particular, se informaron síntomas de TEPT clínicamente significativos en aproximadamente el 30 % de los pacientes con COVID-19 que requirieron hospitalización y pueden presentarse temprano durante la infección aguda o meses después (Mazza, M. G. et al. Brain Behav. Immun. 89, 594–600, 2020; Rogers, J. P. et al. Lancet Psychiatry 7, 611–627, 2020). Un análisis de conjunto de datos a gran escala del mundo real de 62,354 sobrevivientes de COVID-19 de 54 organizaciones de atención médica en los Estados Unidos estimó que la incidencia de la primera enfermedad psiquiátrica y recurrente entre los 14 y 90 días del diagnóstico fue del 18,1 % (Rogers, J. P. et al. Lancet Psychiatry 7, 611–627, 2020). Más importante aún, informó que la probabilidad general estimada de diagnóstico de una nueva enfermedad psiquiátrica dentro de los 90 días posteriores al diagnóstico de COVID-19 era del 5,8 % (trastorno de ansiedad = 4,7 %; trastorno del estado de ánimo = 2 %; insomnio = 1,9 %; demencia (entre los ≥65 años) = 1,6 %) entre un subconjunto de 44.759 pacientes sin enfermedad psiquiátrica previa conocida. Estos valores fueron todos significativamente más altos que en las cohortes de control emparejadas de pacientes diagnosticados con influenza y otras infecciones del tracto respiratorio.
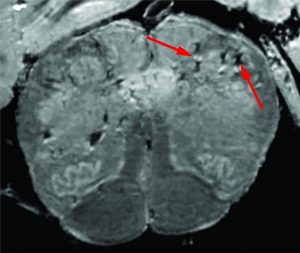
Al igual que en otras enfermedades críticas, las complicaciones del COVID-19 agudo, como el ictus isquémico o hemorrágico (Trejo-Gabriel-Galán, J. M. . Neurologia 35, 318–322, 2020), el daño hipóxico-anóxico, el síndrome de encefalopatía posterior reversible (Parauda, S. C. et al. J. Neurol. Sci. 416, 117019, 2020), y la mielitis aguda diseminada (Ellul, M. A. et al.Ellul, M. A. et al. Lancet Neurol. 19, 767–783, 2020; Paterson, R. W. et al. Brain 143, 3104–3120, 2020), pueden conducir a déficits neurológicos persistentes o permanentes que requieran un extenso rehabilitación. Además, la miopatía y las neuropatías de enfermedad crítica aguda que se producen durante el COVID-19 agudo o por el efecto de los agentes bloqueadores neuromusculares pueden dejar síntomas residuales que persisten durante semanas o meses (Hosey, M. M. & Needham, D. M. Nat. Rev. Dis. Prim. 6, 60, 2020; Tankisi, H. et al. Clin. Neurophysiol. 131, 1931–1932, 2020).
Patología y fisiopatología
Los mecanismos que contribuyen a la neuropatología en COVID-19 pueden agruparse en categorías superpuestas de infección viral directa, inflamación sistémica grave, neuroinflamación, trombosis microvascular y neurodegeneración (Heneka, M. T., et al. Alzheimers Res. Ther. 12, 69, 2020; Muccioli, L. et al. Ann. Neurol. 88, 860–861, 2020; Pilotto, A., Padovani, A. & ENCOVID-BIO Network. Ann, Neurol. 88, 861–862, 2020; South, K. et al. Int J. Stroke 15, 722–732, 2020). Si bien se han informado previamente partículas virales en el cerebro con otras infecciones por coronavirus (Desforges, M., et al. Virus Res. 194, 145–158, 2014), aún no hay evidencia convincente de que el SARS-CoV-2 infecte neuronas. Sin embargo, las series de autopsias han demostrado que el SARS-CoV-2 puede causar cambios en el parénquima cerebral y los vasos, posiblemente por efectos sobre las barreras sangre-cerebro y sangre-líquido cefalorraquídeo, que provocan inflamación en neuronas, células de apoyo y vasculatura cerebral (Romero-Sánchez, C. M. et al. Neurology 95, e1060–e1070, 2020; Reichard, R. R. et al. Acta Neuropathol. 140, 1–6, 2020). Además, los niveles de activación inmunitaria se correlacionan directamente con los cambios cognitivo-conductuales (Bortolato, B., et al. Curr. Neuropharmacol. 13, 558–576, 2015). La inflamación (una inflamación cerebral crónica de bajo nivel), junto con la capacidad reducida para responder a nuevos antígenos y la acumulación de células T de memoria (características de la inmunosenescencia en el envejecimiento y la lesión tisular (Aiello, A. et al. Front. Immunol. 10, 2247, 2019), pueden desempeñar un papel en los efectos persistentes de COVID- 19. Otros mecanismos propuestos incluyen el drenaje linfático disfuncional de los órganos circunventriculares (Perrin, R. et al. Med. Hypotheses 144, 110055, 2020), así como la invasión viral en los espacios extracelulares del epitelio olfatorio y la difusión pasiva y el transporte axonal a través del complejo olfatorio (Morbini, P. et al. JAMA Otolaryngol. Head Neck Surg. https://doi.org/10.1001/jamaoto.2020.2366, 2020). Se han encontrado biomarcadores de lesión cerebral, como niveles elevados de cadena ligera de neurofilamento en sangre periférica, en pacientes con COVID-19 (Ameres, M. et al. J. Neurol. 267, 3476–3478, 2020), con un aumento más sostenido de infecciones graves (Kanberg, N. et al. Neurology https://doi.org/10.1212/WNL.0000000000010111, 2020), lo que sugiere la posibilidad de una lesión neuronal más crónica.
Finalmente, en relación a la niebla mental posterior al COVID, se ha descrito en pacientes críticamente enfermos con COVID-19 puede evolucionar a partir de mecanismos como el desacondicionamiento o el TEPT (Kaseda, E. T. & Levine, A. J. Clin. Neuropsychol. 34, 1498–1514, 2020). Sin embargo, los informes de confusión mental de COVID-19 después de un COVID-19 leve sugieren que la disautonomía también puede contribuir (Novak, P. eNeurologicalSci 21, 100276, 2020; Miglis, M. G., et al. Clin. Microbiol. Infect. https://doi.org/10.1016/j.cmi.2020.08.028, 2020). Por último, el deterioro cognitivo a largo plazo está bien reconocido en el contexto de una enfermedad poscrítica, y ocurre en el 20-40 % de los pacientes dados de alta de una UCI (Sakusic, A. & Rabinstein, A. A. Curr. Opin. Crit. Care 24, 410–414, 2018).
Consideraciones de manejo
Deben implementarse terapias estándar para complicaciones neurológicas como dolores de cabeza, con evaluación por imágenes y derivación a un especialista reservado para la cefalea refractaria (Do, T. P. et al. Neurology 92, 134–144, 2019). Se debe considerar una evaluación neuropsicológica adicional en el contexto de una enfermedad posaguda en pacientes con deterioro cognitivo. Deben utilizarse herramientas de detección estándar para identificar a los pacientes con ansiedad, depresión, trastornos del sueño, trastorno de estrés postraumático, disautonomía y fatiga (George, P. M. et al. Thorax 75, 1009–1016, 2020; Kaseda, E. T. & Levine, A. J. Clin. Neuropsychol. 34, 1498–1514, 2020).

